Los carbonatos ( CO3 -2) son sales que resultan de la combinación del ácido carbónico -o un éster carbónico- y un metal. Una o más moléculas de hidrógeno del ácido son sustituidas por el metal base, formando así el compuesto químico. Los cationes del metal establecen el enlace iónico con los aniones del ácido carbónico.
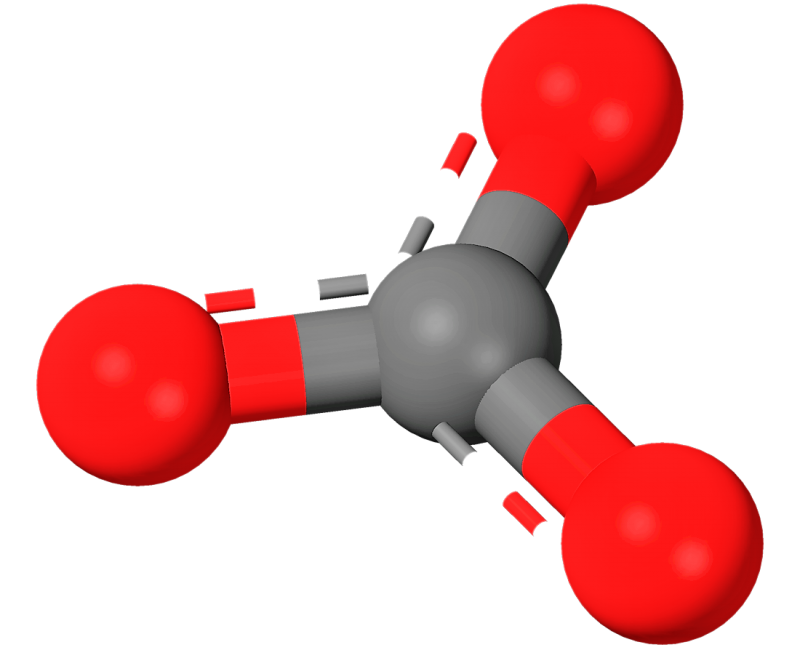
En el ion carbonato los tres enlaces de C-O son idénticos y 2/3 comparten la carga negativa a través de enlaces parciales (entre simples y dobles). Los carbonatos se clasifican en grupos isoestructurales, correspondientes a los sistemas trigonal y rómbico. Al primero pertenecen los grupos de la calcita y de la dolomita; al sistema rómbico, el grupo del aragonito. También pueden dividirse en carbonato anhidros e hidratados.
El éster carbónico se considera un derivado del ácido carbónico y se caracteriza por el grupo funcional R1-O-CO-O-R2. En el enlace dos moléculas de hidrógeno son sustituidas por radicales. Los compuestos de este grupo son denominados carbonatos de…(el nombre del radical de alquilo). Entre los más conocidos se encuentran los carbonatos de dimetilo y de etibutilo.
Clasificación
Los carbonatos anhidros e hidratados han sido clasificados en grupos isoestructurales. Según su estructura cristalina y composición química se dividen en:
Anhidros
- Grupo de la calcita: Integrado por el carbonato de calcio, carbonato cálcico o creta (CaCO3). También por los carbonatos de magnesita (MgCO3), de siderita (mineral de hierro FeCO3), y de rodocrosita o manganeso (MnCO3). La smitsonita, carbonato de zinc (ZnCO3), pertenece igualmente a este grupo del sistema cristalino trigonal.
- Grupo de la dolomita: Lo conforma la dolomita, carbonato de calcio y magnesio CaMg (CO3)2; y la ankerita CaFe2+ (CO3)2. Ambas de sistema cristalino trigonal.
- Grupo del aragonito: El carbonato de aragonito es la presentación cristalina del carbonato de calcio y comparte la misma fórmula química CaCO3. Integran también el grupo, la witherita o carbonato de bario (BaCO3), estroncianita (SrCO3) y cerucita o carbonato de plomo (PbCO3).
Básicos o hidratados
Los más comunes en esta categoría son los carbonatos de cobre: Malaquita (Cu2 CO3 (OH)2) y la azurita (Cu3 CO3 (OH)2). Más pertenecen al grupo el natrón, lantanita, lansfordita, termonatrina y la hidromagnesita, entre otros.
Importancia y uso de los carbonatos
Los carbonatos son compuestos químicos abundantes en la naturaleza, tienen una alta capacidad de neutralización y múltiples usos en la industria. Los de mayor presencia en la superficie terrestre y además los más utilizados son el carbonato de calcio y el de dolomita. Tienen tantas o más aplicaciones que el cuarzo y las arcillas.
El carbonato cálcico es materia prima en la elaboración del papel, vidrio, cerámica y cemento. Es útil en pinturas, adhesivos, hules, cauchos y plásticos, en jabones y detergentes. Es preferido por su accesible costo en relación a otros compuestos, su alto grado de blancura y pureza, así como su buena dispersabilidad.
Las rocas calizas y dolomías, ricas en estos compuestos, se emplean en procesos de oxidación atmosférica. También en la desulfuración en la industria metalúrgica y más comúnmente, en la descontaminación y preparación de los suelos. Mientras que los carbonatos de zinc, anhidros o hidratados, tienen su lugar en la industria farmacéutica.
Menas de metales
Algunos de los carbonatos son lo suficientemente abundantes para servir de mena de los metales base, tal es el caso de la siderita. El también conocido como espato de hierro, es un carbonato ferroso que se origina a partir de procesos magmáticos y de alteración. Aunque carece de valor petrogénico es buena fuente de hierro. Las rocas de magnesita son menas de magnesio.
Los sulfuros de plomo, cobre y zinc también son abundantes en las formaciones carbonatadas, especialmente en los yacimientos alpinos. Las mineralizaciones metálicas tienen origen sedimentario, aunque algunas se han detectado posterior a los depósitos. Un ejemplo de mineralización post sedimentaria lo ofrecen las dolomías, menas también de magnesio.
Desde el punto de vista de la geología y la minería, los compuestos químicos carbonatos son de gran importancia. No sólo concentran metales, también agua, petróleo e inclusive gas.
Yacimientos de carbonatos
Los yacimientos de minerales carbonatados más conocidos se ubican en Europa, Oriente Medio y Norteamérica. El desarrollo y factibilidad económica de estas explotaciones dependen de factores como la diagénesis, frecuencia estratigráfica y la fracturación.
El carbonato cálcico está presente en forma de bicarbonato en las aguas naturales, esto por acción del anhídrido carbónico. Cuando éste último falta, el carbonato cálcico forma estalagmitas y estalactitas, entre otros tipos de depósitos. Es además componente primario de la cal agrícola.
El carbonato de magnesio se consigue en forma de sal anhidra o magnesita, dihidrato barringtonita y trihidrato nesquehonita. También como lansfordita, artinita e hidromagnesita. La sal anhidra es insoluble en agua y otros agentes químicos. Las demás presentaciones se disuelven en ácidos fuertes y a determinadas temperaturas.
























Deja una respuesta